https://edis.ifas.ufl.edu/publication/EP546

IL DESTINO DELL'AZOTO APPLICATO AL TAPPETO ERBOSO DELLA FLORIDA
TW Shaddox e JB Unruh
La qualità delle acque superficiali e sotterranee della Florida è della massima importanza per la flora e la fauna che vivono in queste acque. La crescita della flora e della fauna è direttamente correlata alla quantità di nutrienti disponibili in queste acque. Inoltre, utilizziamo queste acque come fonte primaria di acqua potabile per noi stessi e le nostre famiglie. In queste acque si può trovare un'ampia gamma di composti, il più comune dei quali può essere il nitrato (NO 3 - ) (Pye et al. 1983). Le fonti di azoto (N) possono includere, ma non sono limitate a, deposizione atmosferica (National Atmospheric Deposition Program 2015), fosse settiche (Katz et al. 2010), smaltimento delle acque effluenti (Warneke et al. 2011), fertilizzazione agricola ( Schmidt e Clark 2012), o la fertilizzazione del paesaggio (Erickson et al. 2008). Nonostante le prove contrarie, alcuni abitanti della Florida presumono che l’azoto applicato ai tappeti erbosi sia uno dei principali responsabili dell’inquinamento idrico (Shaddox et al. 2016a; Shaddox et al. 2016b; Telenko et al. 2015; Trenholm e Unruh 2005). Al fine di prendere decisioni informate riguardo alle applicazioni di N sul tappeto erboso, è importante comprendere il ciclo dell'N nel sistema suolo/tappeto erboso. Pertanto, l'obiettivo di questa pubblicazione è identificare e descrivere le fonti e i potenziali destini dell'N applicato al tappeto erboso della Florida.
Questa discussione includerà cinque percorsi che N può intraprendere dopo essere stato applicato al tappeto erboso: conversione in gas atmosferico, assorbimento del tappeto erboso, stoccaggio nel suolo, lisciviazione e deflusso. Tuttavia, è importante comprendere innanzitutto il contributo del tappeto erboso al consumo di fertilizzanti della Florida. Quando discutiamo della qualità dell'acqua della Florida, in particolare della contaminazione da N, dobbiamo considerare tutte le potenziali fonti di N e il loro relativo contributo alla contaminazione delle acque sotterranee. La Florida è posizionata in modo unico in un ambiente con luce solare, precipitazioni e temperatura ottimali, che consente la crescita delle piante e la produzione agricola tutto l'anno. L’aumento della crescita delle piante è spesso una funzione delle applicazioni di N. Le applicazioni di azoto sono considerate essenziali per sostenere la produzione alimentare necessaria al sostentamento della nostra popolazione. Se si considera tutto il fertilizzante N applicato in Florida, la quantità applicata al tappeto erboso è relativamente bassa, contribuendo solo per l’11% all’N totale applicato in Florida (FDACS 2017). Sebbene tale percentuale sia bassa rispetto ad altri mercati, è comunque fondamentale comprendere i percorsi che potrebbe intraprendere in un sistema a tappeto erboso. Comprendere questi destini aiuterà a proteggere l'ecosistema della Florida e a migliorare le decisioni relative alle migliori pratiche di gestione.
AZOTO ATMOSFERICO
Più del 99% di tutto l'azoto presente sul pianeta terra esiste nell'atmosfera (Havlin et al. 1999) ed è chimicamente e biologicamente non disponibile per le piante, ad eccezione di quelle capaci di fissazione biologica dell'azoto. Circa il 78% dell'aria che respiriamo è gas N2, che può essere convertito in una forma utilizzabile (ad esempio fertilizzante) tramite il processo Haber-Bosch o mediante fissazione biologica dell'azoto. Circa l’80% dell’azoto prodotto tramite il processo Haber-Bosch viene utilizzato per fertilizzanti agricoli (Galloway et al. 2008) e si stima che il processo Haber-Bosch sia responsabile della fornitura dei bisogni alimentari del 50% della popolazione umana ovvero 3 miliardi di persone (Smil 2001). Pertanto, dopo la fotosintesi, il processo Haber-Bosch potrebbe essere il processo più importante che ha influenzato lo sviluppo umano nel secolo scorso (Erisman et al. 2008). Una volta raccolto dall'atmosfera, l'N applicato al tappeto erboso si converte facilmente in gas tramite volatilizzazione o denitrificazione (Figura 1).

Figura 1. Il ciclo dell'azoto nel tappeto erboso.
Credito: Travis Shaddox, UF/IFAS
La volatilizzazione è la conversione di N in ammoniaca (Figura 2). I fattori che influenzano la conversione di N in un gas includono la quantità di N solubile come urea o ammonio, temperatura, pH elevato del terreno, bassa umidità del suolo e bassa capacità di scambio cationico. L'azoto convertito in ammoniaca viene disperso nell'atmosfera e non è più disponibile per l'assorbimento del tappeto erboso. Sebbene la volatilizzazione sia un netto svantaggio per il tappeto erboso, la perdita di N sotto forma di ammoniaca diminuisce la quantità di N disponibile per spostarsi nei corpi idrici vicini tramite lisciviazione o deflusso. Tuttavia, la volatilizzazione dell’N può aumentare la quantità di N restituito alla terra attraverso le precipitazioni e la deposizione atmosferica. Poiché l’N è comunemente applicato al tappeto erboso come urea, la volatilizzazione può essere uno dei principali fattori che contribuiscono alla perdita di N dai sistemi a tappeto erboso, con perdite che vanno da <1% fino al 60% dell’N applicato (Goos 2011). Questa percentuale può essere ridotta utilizzando urea a lento rilascio, inibitori dell’ureasi o irrigando il tappeto erboso immediatamente dopo la fertilizzazione (Franzen et al. 2011). Le fonti di N a rilascio lento sono definite come qualsiasi fonte di N che rilascia il suo N a una velocità più lenta rispetto a una fonte di N solubile di riferimento (AAPFCO 2017). Gli inibitori dell'ureasi rallentano la conversione dell'urea in NH4+ inibendo l'ureasi, l'enzima necessario affinché avvenga l'idrolisi dell'urea. In tal modo, il tasso di volatilizzazione può essere ridotto fino alla metà (Goos 2011). Gli inibitori dell'ureasi possono essere commercializzati come "stabilizzatori dell'azoto". Numerosi prodotti commercializzati come inibitori dell'ureasi sono stati testati da istituti di concessione di terreni. Solo gli "stabilizzatori dell'azoto" contenenti triammide dell'acido N-(n-butil) tiofosforico (NBPT) o triammide dell'acido N-(n-propil) tiofosforico (NPPT) hanno una volatilizzazione costantemente ridotta rispetto alla sola urea (Franzen et al. 2011; Goos 2011). Anche il fertilizzante azotato a rilascio lento ha ridotto la volatilizzazione non attraverso l’inibizione dell’ureasi, ma ritardando il rilascio dell’urea nel ciclo dell’azoto.
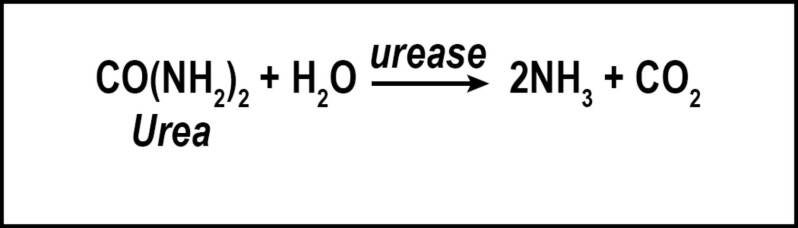
Figura 2. La volatilizzazione dell'azoto converte l'urea in gas di ammoniaca.
Credito: Travis Shaddox, UF/IFAS
La denitrificazione è la conversione microbica del gas NO3 in N2 (Figura 3). Le condizioni che favoriscono la denitrificazione sono terreni umidi e organici contenenti NO3- (Galloway et al. 2004). Simile alla volatilizzazione, la denitrificazione converte N in una delle numerose specie N: nitrito (NO2-), ossido nitrico (NO), protossido di azoto ( N2O) o N gassoso (N2), riducendo la quantità di N disponibile per le piante e la quantità di N disponibile per spostarsi verso posizioni non target. La denitrificazione richiede che l'N sia nella forma NO3, che viene poi ridotta quando l'ossigeno viene rimosso. La denitrificazione è fortemente influenzata dall’aumento dell’umidità del suolo, che si traduce in un terreno privo di ossigeno e accelera la rimozione dell’ossigeno da NO3- da parte dei batteri denitrificanti. Quando i livelli di ossigeno nel suolo scendono al di sotto del 2%, la denitrificazione aumenta. Tuttavia, la denitrificazione può ancora verificarsi in suoli aerati a causa della saturazione dei micrositi interni del suolo (Carrow et al. 2001). Gli studi sul tappeto erboso progettati per determinare i tassi di denitrificazione in Florida sono limitati. Tuttavia, nei terreni sabbiosi e ben drenati, la denitrificazione è normalmente bassa e rappresenta da <1% a 5% dell'N applicato, ma potrebbe avvicinarsi al 94% quando la temperatura supera i 30°C (Mancino et al. 1988). La denitrificazione nei sistemi di tappeti erbosi è paragonabile ad altri agroecosistemi in cui il 10–40% dell'N applicato può essere denitrificato (Galloway et al. 2004). Sebbene sia già bassa nei sistemi di tappeti erbosi della Florida, la denitrificazione può essere ulteriormente ridotta utilizzando inibitori della nitrificazione o N a lento rilascio, che possono ridurre la quantità di NO3-N nel terreno. Gli inibitori della nitrificazione dovrebbero contenere 2-cloro-6(triclorometil) piridina (Nitrapyrin) o diciandiammide (DCD), poiché questi sono gli unici due composti che hanno ridotto la denitrificazione negli studi sul campo e in laboratorio (Janzen e Bettany 1986; Malzer 1989; Malzer et al.1989). Analogamente al loro effetto sulla volatilizzazione, i fertilizzanti azotati a lento rilascio possono ridurre la denitrificazione ritardando il rilascio del loro azoto nel ciclo dell’azoto. Sono necessarie ulteriori ricerche volte a determinare i tassi di denitrificazione nei sistemi di tappeti erbosi della Florida.
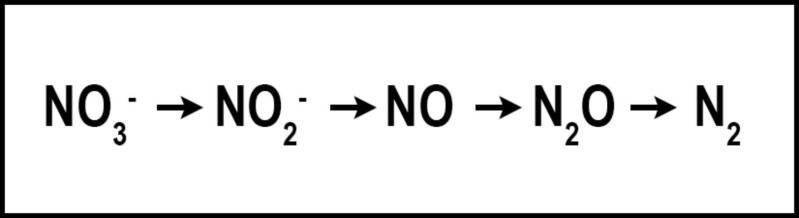
Figura 3. Denitrificazione - NO 3 -N è soggetto a riduzione da parte dei microbi del suolo, portando a N 2 .
Credito: Travis Shaddox, UF/IFAS
ASSORBIMENTO DEL TAPPETO ERBOSO
L'obiettivo di tutte le applicazioni di N sul tappeto erboso è l'assorbimento sostenibile da parte delle piante e il conseguente aumento della crescita o della qualità del tappeto erboso. Numerosi fattori possono influenzare l’assorbimento di N da parte del tappeto erboso, tra cui (ma non limitati a) specie di tappeto erboso, stagione, tipo di N, tasso di N e gestione dell’umidità.
La percentuale di N applicato recuperato nel tessuto del tappeto erboso può variare a seconda della specie del tappeto erboso. Le specie che possiedono una maggiore densità di radici più in profondità nel profilo del suolo tendono ad assorbire maggiori quantità di N applicato rispetto ai tappeti erbosi con sistemi radicali meno densi (Bowman et al. 2002). Chiaramente, un maggiore assorbimento si verifica perché un tappeto erboso con una maggiore quantità di radici ha una maggiore possibilità che le sue radici intercettino e assorbano N (Sullivan et al. 2000). È stato documentato che la St. Augustinegrass e la bermudagrass (due delle erbe più comuni in Florida) utilizzano percentuali maggiori di N applicato rispetto al centopiedi, alla bahiagrass e alla zoysiagrass (Bowman et al. 2002). Anche le cultivar della stessa specie possono differire nella capacità di consumare l’azoto applicato (Young 2015). Sebbene la causa esatta non sia completamente nota, è ragionevole postulare che le differenze tra le cultivar siano dovute a diversi livelli di evapotraspirazione (ET), produzione di sostanza secca o masse radicali, che comporterebbero il consumo di diverse quantità di N applicato.
Come per la maggior parte delle piante, il cambiamento delle stagioni climatiche può avere un’influenza drammatica sulla crescita delle piante e sull’assorbimento dei nutrienti. Durante l'inverno nel nord della Florida, la maggior parte dei tappeti erbosi della stagione calda mostrerà una diminuzione della crescita e potrebbe entrare in dormienza (una fase naturale del tappeto erboso in cui la pianta è viva, ma non si verifica alcuna divisione cellulare o allungamento). Anche nel sud della Florida, durante l'inverno si verificherà una crescita ridotta del tappeto erboso, ma non è stata segnalata una vera dormienza. Quando la crescita del tappeto erboso diminuisce, diminuisce anche la quantità di N necessaria al tappeto erboso. Pertanto, il consumo di N applicato può essere inferiore in inverno che in estate (Wherley et al. 2009). Le applicazioni di N su tappeti erbosi dormienti o semi-dormienti non hanno comportato la lisciviazione di N a meno che non si verifichino precipitazioni eccessive (Shaddox et al. 2016a); pertanto, l’azoto applicato rimarrà nel terreno finché la pianta non lo consumerà o finché la pioggia/irrigazione non sposterà l’azoto oltre la zona radicale (Wherley et al. 2009). Tuttavia, i vantaggi agronomici derivanti dall’applicazione di N ai tappeti erbosi dormienti sono bassi rispetto al rischio ambientale. Pertanto, le applicazioni di N sui tappeti erbosi dormienti in Florida non sono raccomandate.
I fertilizzanti azotati differiscono nella forma di N e nelle caratteristiche di rilascio. Queste differenze possono portare a diverse quantità di N assorbito dal tappeto erboso. L'azoto applicato come NH 4 + può comportare un assorbimento inferiore di N rispetto a quello applicato come NO 3 - a causa della tendenza dell'NH 4 + a volatilizzarsi e ad essere perso dal sistema terreno/tappeto erboso (Brown 2003). Una percentuale maggiore di N proveniente da fertilizzanti a lenta cessione può essere assorbita dal tappeto erboso rispetto alle fonti di N solubili (Shaddox 2001). L’azoto solubile è immediatamente disponibile per seguire qualsiasi percorso potenziale nel sistema terreno/tappeto erboso, compresa la lisciviazione e la volatilizzazione, mentre solo piccole porzioni di azoto provenienti dai fertilizzanti a rilascio lento diventano solubili in un dato momento. A tal fine, i fertilizzanti a lenta cessione di N possono aumentare l’assorbimento di N fino al 300% rispetto alle fonti di N solubili (Shaddox 2001).
Un fattore trainante alla base delle raccomandazioni sui nutrienti UF/IFAS per il tappeto erboso è quello di applicare la quantità di N necessaria per ottenere la risposta desiderata del tappeto erboso senza applicare più N di quanto il tappeto erboso può consumare in un dato momento. Quando si seguono i tassi di N raccomandati da UF/IFAS, l'assorbimento dell'N applicato dal tappeto erboso varia dal 40 al 68% (Brown 2003; Sartain 1985; Shaddox 2001; Stiegler et al. 2011), mentre la ricerca condotta al di fuori della Florida indica che la percentuale di assorbimento può avvicinarsi 80% (Bowman et al. 2002). Quando vengono applicate piccole quantità di N, solo una minima parte di N ha la possibilità di sfuggire all'assimilazione del tappeto erboso. All’aumentare dei tassi di N solubile, la percentuale di N applicato recuperata nei tessuti del tappeto erboso diminuisce (Ashley et al. 1965). Tuttavia, le fonti di N a lento rilascio spesso richiedono tassi di applicazione più elevati rispetto alle fonti di N solubili per ottenere la stessa risposta desiderata del tappeto erboso, perché solo una piccola parte dell’N a lento rilascio diventerà solubile su base giornaliera. Di conseguenza, tassi più elevati di fonti di N a lento rilascio possono comportare un assorbimento percentuale maggiore di N applicato rispetto a tassi più bassi (Sartain 1985). Inoltre, una singola applicazione di N a rilascio lento ad una velocità elevata può comportare lo stesso assorbimento di N dell’N solubile applicato come applicazione frazionata (Sartain 2008). Pertanto, le fonti di N a lento rilascio possono essere applicate a tassi più elevati rispetto alle fonti di N solubile purché il tasso di applicazione singolo e il totale annuo di N applicato non superino le raccomandazioni UF/IFAS.
La gestione dell'umidità influenza notevolmente l'assorbimento da parte delle piante dell'azoto applicato. La maggior parte dell'azoto viene assorbito dalla pianta attraverso la soluzione del terreno. Pertanto, quando il contenuto di acqua del suolo supera la capacità di ritenzione idrica del suolo, l’N nella soluzione del suolo può essere spostato al di sotto della zona radicale, il che si traduce in un ridotto assorbimento da parte delle piante (Shaddox, 2001). D'altra parte, quando viene applicata una quantità d'acqua insufficiente, il tappeto erboso può entrare in uno stato di dormienza indotto dalla siccità in cui riduce l'assorbimento di acqua e azoto per sopravvivere (Ashley et al. 1965). Pertanto, dovrebbe essere prestata un'attenta considerazione all'applicazione di acqua sufficiente per mantenere il tappeto erboso accettabile, ma non all'applicazione di più acqua di quella che può essere trattenuta dal terreno. In generale, il sensore pioggia, il sensore dell’acqua del suolo e i controllori dell’evapotraspirazione applicano l’acqua in modo più efficace rispetto ai controllori temporizzati automaticamente (Dobbs et al. 2014).
RITENZIONE DEL SUOLO, IMMOBILIZZAZIONE E FISSAZIONE DI NH 4 +
La quantità di N immagazzinata nel suolo dipende da molti fattori, in particolare dal tipo di fertilizzante, dalla quantità di fertilizzante, dal periodo dell'anno, dall'umidità del suolo, dal pH del suolo e dalle precipitazioni. La maggior parte dell'N del suolo esiste come N organico sotto forma di sostanza organica o come N che non è stato rilasciato dai granuli di fertilizzante a lenta cessione. Tecnicamente, i granuli di fertilizzante non sono un componente dell’N immagazzinato nel suolo. Tuttavia, il processo di misurazione dell’N del suolo (combustione o digestione) misurerà anche l’N da eventuali granuli di fertilizzante che non sono ancora stati rilasciati. Il tipo e la quantità di fertilizzante a lenta cessione influenzeranno direttamente questo valore. Una volta rilasciato dalla forma a rilascio lento, l’N può rimanere nel terreno tramite scambio anionico o cationico. La capacità di scambio cationico della maggior parte dei suoli della Florida è normalmente inferiore a 3 milliequivalenti di carica positiva e la capacità di scambio anionico è normalmente troppo bassa per essere misurata. Nei terreni della Florida, l'N mineralizzato, l'N applicato come urea, o l'N applicato come NH 4 + possono rapidamente convertirsi in NO 3 - e, poiché NO 3 - è un anione, non viene trattenuto dal suolo. Pertanto, l’immagazzinamento di N nel suolo attraverso lo scambio cationico è comunemente inferiore al 10% dell’N applicato (Shaddox 2001) e può essere inferiore al 2% (Brown 2003).
L'immobilizzazione dell'azoto avviene quando l'N inorganico viene convertito in N organico attraverso l'attività microbica. Una forma organica di N è semplicemente qualsiasi forma di N legata al carbonio. Come le piante, i microbi richiedono N per sopravvivere e una parte dell’N applicato verrà consumata dai microbi e convertita in amminoacidi, proteine o qualche altra forma organica utilizzata per la crescita dai microbi. Mentre si trova in forma organica, l'N non è solubile e pertanto non è disponibile per l'assorbimento o la perdita da parte delle piante in un corpo idrico. L’azoto organico rimarrà non disponibile per l’assorbimento da parte delle piante finché le condizioni ambientali non cambieranno per favorire la mineralizzazione dell’azoto. La percentuale di N applicato che viene immobilizzato microbicamente nei sistemi di tappeto erboso della Florida varierà in base a numerosi fattori tra cui l’umidità del suolo, il pH e la temperatura del suolo. Sono state condotte poche, se non nessuna, ricerche per determinare l'immobilizzazione dell'N applicato nei sistemi di tappeti erbosi della Florida. Pertanto, fornire una stima è difficile. Tuttavia, ricerche condotte su tappeti erbosi in climi più freddi (Connecticut) riportano che l’immobilizzazione di N può variare dal 15 al 26% dell’N applicato (Starr e Deroo 1981). Poiché la Florida riceve più precipitazioni ed è più calda del Connecticut, l’immobilizzazione di N in Florida potrebbe essere inferiore a quanto indicato da precedenti rapporti a causa dell’aumento dell’attività microbica.
La fissazione dell'ammonio avviene quando NH 4 + entra nello strato (reticolo) di un'argilla 2:1 (Figura 4), diventando non disponibile per l'assorbimento da parte delle piante. Si ritiene che la fissazione dell'ammonio nei suoli della Florida contribuisca molto poco al destino complessivo dell'azoto applicato per due ragioni. In primo luogo, il contenuto di argille 2:1 nei suoli della Florida è normalmente molto basso e, in secondo luogo, NH 4 + normalmente si converte in NO 3 - molto rapidamente. La percentuale esatta di N applicato ai tappeti erbosi della Florida che alla fine viene fissata da minerali argillosi 2:1 non è nota. Tuttavia, prove provenienti da altri sistemi agronomici indicano che la percentuale è inferiore al 5% (Nieder et al. 2011).

Figura 4. L'ammonio può fissarsi all'interno del reticolo delle argille 2:1 ed essere reso non disponibile per l'assorbimento del tappeto erboso.
Credito: modificato da Strand (1998)
LISCIVIAZIONE
La lisciviazione è il processo che sposta l'N solubile al di sotto della zona radicale. La lisciviazione dell'azoto nei sistemi di tappeti erbosi avviene nel momento in cui l'azoto solubile si sposta al di sotto della radice più profonda. Quando il tappeto erboso viene fertilizzato secondo le raccomandazioni UF/IFAS, la lisciviazione di N è normalmente bassa e paragonabile, o inferiore, a quella di altre piante paesaggistiche (Erickson et al. 2008). Come per altri destini dell'azoto applicato, la quantità esatta di azoto che verrà lisciviato è difficile da determinare. Tuttavia, è possibile che dallo 0 al 55% dell'azoto applicato venga disciolto, con percentuali più elevate che si verificano quando non vengono seguite le raccomandazioni UF/IFAS. Quando si verifica la lisciviazione di N, di solito è un fattore legato alla specie del tappeto erboso, alla gestione dell’irrigazione, alla fonte di N, al tasso di N o al tappeto erboso stressato.
Confronti diretti di N perso attraverso la lisciviazione relativa alle specie di erba da tappeto erboso indicano che meno N liscivia attraverso la erba di St. Augustine 'Raleigh' rispetto alla zoysiagrass 'Empire', alla zoysiagrass 'Meyer', alla zoysiagrass 'Emerald', al millepiedi, alla bermudagrass 'Tifway' e alla bermudagrass comune ( Bowman et al. 2002; Telenko et al. 2015; Trenholm et al. 2012). L’influenza delle specie del tappeto erboso sulle perdite per lisciviazione di N è in gran parte un fattore legato al sistema radicale del tappeto erboso. I tappeti erbosi con radici più profonde tendono a ridurre le perdite per lisciviazione di N rispetto ai tappeti erbosi con radici poco profonde (Bowman et al. 1998). Le pratiche di gestione che incoraggiano il radicamento profondo, come l’irrigazione profonda e poco frequente, sono fattori che modellano le raccomandazioni UF/IFAS. È stato documentato un aumento della lisciviazione di N quando l’N viene applicato entro i primi 60 giorni dalla piantumazione della zolla (Telenko et al. 2015). Dopo che la zolla è stata piantata per 60 giorni, la lisciviazione di N è ridotta ed è il risultato di una maggiore crescita delle radici. Sulla base di questi risultati, UF/IFAS raccomanda che le applicazioni di N sul tappeto erboso appena interrato inizino 60 giorni dopo che la zolla è stata piantata. Questa raccomandazione consente alla zolla di sviluppare un apparato radicale prima della fertilizzazione e quindi minimizza il rischio di lisciviazione di N.
Il movimento dell'acqua attraverso il suolo ha una profonda influenza sulla lisciviazione dell'azoto. Una volta che un nutriente diventa solubile nella soluzione del terreno, quel nutriente è soggetto al movimento dell'acqua. Pertanto, è fondamentale ridurre al minimo qualsiasi movimento di acqua oltre la zona radicale del tappeto erboso. L’aumento del movimento dell’acqua può essere il risultato di un’irrigazione eccessiva o delle fluttuazioni delle precipitazioni dovute al cambiamento delle stagioni, che possono comportare l’applicazione al terreno di una quantità di acqua superiore a quella che il suolo può trattenere. Il sensore di umidità o l'irrigazione basata su ET sono più efficaci dell'irrigazione giornaliera nell'applicare la quantità di acqua di cui il tappeto erboso ha bisogno senza superare la capacità di ritenzione idrica della zona radicale. Durante tutto l’anno, la lisciviazione di N può essere massima in febbraio-marzo, ridotta in aprile-maggio e minima in giugno-luglio (Snyder et al. 1984). La riduzione della lisciviazione di N dall’inverno all’estate è in gran parte un fattore di maggiore crescita delle piante e di aumento di ET, che riducono rispettivamente la quantità di N nella soluzione del suolo e la quantità di umidità nella zona radicale. In ogni stagione, l’irrigazione basata su sensori può ridurre la lisciviazione di N da 2 a 28 volte rispetto all’irrigazione giornaliera. Pertanto, l'UF/IFAS raccomanda di astenersi dall'applicare qualsiasi N quando il Servizio meteorologico nazionale ha emesso un'alluvione, una tempesta tropicale o un avviso o un avviso di uragano, o se sono probabili forti piogge. Queste raccomandazioni riducono il rischio di superare la capacità di ritenzione idrica del suolo e, di conseguenza, riducono la lisciviazione di N.
Se applicato secondo le raccomandazioni UF/IFAS, l'N solubile potrebbe non lisciviare più N rispetto all'N perso naturalmente dal tappeto erboso non fertilizzato (Shaddox et al. 2016a). Inoltre, le fonti di N a lento rilascio riducono ulteriormente le perdite per lisciviazione di N rispetto alle fonti di N solubili. Essenzialmente, le fonti di N a rilascio lento ritardano il rilascio di N nel ciclo dell'N (Figura 1). Nel corso del tempo, vengono rilasciate piccole porzioni di N, il che aumenta la probabilità di assorbimento dell’N applicato da parte delle piante e diminuisce il rischio di perdite per lisciviazione di N (Guillard e Kopp 2004). Anche la miscelazione di fonti di N solubili con fonti di N a rilascio lento determina perdite ridotte per lisciviazione di N (Shaddox 2001). In generale, le differenze nelle perdite per lisciviazione di N tra le fonti di N a lento rilascio sono trascurabili presupponendo che vengano applicate allo stesso tempo e allo stesso tasso. Tuttavia, le fonti di N organico e le fonti di N rivestite con polimeri possono comportare una quantità minore di perdite per lisciviazione di N rispetto ad altre fonti a lento rilascio (Petrovic 2004). I fertilizzanti ad efficienza migliorata, come la nitrificazione e gli inibitori dell’ureasi, non ritardano il rilascio di N nel ciclo dell’azoto e quindi comportano perdite per lisciviazione di N simili a quelle di altre fonti di N solubili (Guertal e Howe 2012).
Aumentare il tasso di N applicato oltre il tasso raccomandato da UF/IFAS ( https://edis.ifas.ufl.edu/publication/ep353 ) può aumentare il rischio di perdite per lisciviazione di N (Trenholm et al. 2012). Le raccomandazioni sui nutrienti per il tappeto erboso UF/IFAS tengono conto del fabbisogno di N del tappeto erboso e del potenziale impatto sull'ambiente. Le raccomandazioni sui nutrienti UF/IFAS sono spesso inferiori del 50–75% rispetto alla quantità di N necessaria per aumentare le perdite per lisciviazione di N al di sopra dell’ambiente naturale (McGroary et al. 2017; Trenholm et al. 2012). Pertanto, i tassi attuali sono considerati conservativi e il superamento di questi tassi non è necessario perché qualsiasi ulteriore aumento della crescita o della qualità del tappeto erboso è minimo e potrebbe comportare un costo per l’ambiente.
Come accennato in precedenza, l’N applicato secondo le raccomandazioni UF/IFAS su tappeti erbosi sani e in crescita ha una bassa probabilità di lisciviazione. Tuttavia, quando il tappeto erboso è stressato, la lisciviazione di N può aumentare (Telenko et al. 2015). Normalmente, gli stress si manifestano come riduzioni della densità e della crescita del tappeto erboso, che corrispondono ad una riduzione dell’assorbimento di N. Questi stress sono in gran parte causati dall’ambiente, da parassiti, gelate di fine stagione e cambiamenti di stagione. Tuttavia, lo stress può anche essere di origine antropica causato da un’errata applicazione di nutrienti o prodotti per il controllo dei parassiti. Quando si verificano stress, ulteriori applicazioni di N potrebbero non risolvere il problema ma, di fatto, potrebbero esacerbare il problema e aumentare la lisciviazione di N. Sono necessarie ulteriori ricerche su come gestire le applicazioni di nutrienti sui tappeti erbosi stressati.
DEFLUSSO
Il deflusso è definito come il movimento laterale di N oltre la posizione target. Il deflusso può avvenire sopra o sotto la superficie del suolo, ma avviene sempre sopra la radice più profonda. Nel momento in cui N si sposta al di sotto della radice più profonda, l'ulteriore spostamento di N è definito lisciviazione. L'N lisciviato può quindi defluire se incontra una barriera sotterranea, ma l'N perso dal sistema del tappeto erboso è considerato lisciviato se l'N si è spostato verticalmente oltre la zona radicale. L'azoto perso tramite il deflusso può essere influenzato dalla topografia, dal tipo di terreno, dalla compattazione del suolo, dall'umidità del suolo, dalle precipitazioni e dal tipo di fertilizzante. Poiché i terreni della Florida sono prevalentemente sabbiosi e hanno un’elevata capacità di infiltrazione dell’acqua, il movimento dell’acqua attraverso la superficie del suolo è molto meno comune del movimento dell’acqua nel suolo. Pertanto, in Florida, gli studi sul deflusso sono meno comuni degli studi sulla lisciviazione perché i pochi studi sul deflusso esistenti riportano che si verifica un deflusso minimo o nullo. In Florida, quando l’azoto viene applicato su pendii ripidi soggetti a tassi di irrigazione intensi, è stato riportato che l’azoto trovato nel deflusso è inferiore allo 0,1% di quello applicato (Shaddox e Sartain 2001). Questa evidenza non esclude la probabilità che il deflusso possa verificarsi in condizioni diverse. Tuttavia, anche su suoli meno permeabili rispetto a molti suoli presenti in Florida, il deflusso di N dal tappeto erboso è comunemente pari allo 0% dell’N applicato, ma può avvicinarsi al 7% su topografie e ambienti non comuni in Florida (Brown et al. 1977; Morton et al. .1988).
RIEPILOGO
Il destino dell'N applicato al tappeto erboso della Florida può variare notevolmente a seconda di numerosi fattori. Essenzialmente tutto l’azoto utilizzato nella gestione del tappeto erboso ha origine dall’atmosfera e alla fine ritornerà nell’atmosfera. Durante questo ciclo, gli intervalli dei potenziali destini dell'N applicato ai tappeti erbosi della Florida sono:
-
Volatilizzazione—<1%–60%
-
Denitrificazione—<1%–5%
-
Assorbimento da parte delle piante —40%–68%
-
Stoccaggio nel suolo: 7%–15%
-
Lisciviazione—<1%–55%
-
Deflusso—<1%–7%
RIFERIMENTI
Ashley, DA, OL Bennett, BD Doss e CE Scarsbrook. 1965. "Effetto del tasso di azoto e dell'irrigazione sulla resa e sul recupero dell'azoto residuo da parte delle erbe della stagione calda". Agron. J . 57: 370–372.
Associazione americana dei funzionari americani per il controllo degli alimenti vegetali. 2017. Pubblicazione ufficiale. Associazione dei funzionari americani per il controllo degli alimenti vegetali, Inc., West Lafayette, IN.
Bowman, DC, CT Cherney e TW Rufty. 2002. "Destino e trasporto dell'azoto applicati a sei tappeti erbosi della stagione calda". Ritaglia Sci. 42:833–841.
Bowman, DC, DA Devitt, MC Engelke e TW Rufty. 1998. "L'architettura delle radici influisce sulla lisciviazione dei nitrati dal tappeto erboso dell'erba piegata". Ritaglia Sci . 38:1633–1639.
Brown, EA 2003. "Lisciviazione differenziale di nitrati e bilancio di massa di 15 fonti di azoto marcate con N applicate a tappeti erbosi e agrumi". Dottorato di ricerca diss., Università della Florida, Gainesville, FL.
Brown, KW, RL Duble e JC Thomas. 1977. "Influenza della gestione e della stagione sul destino di N applicato ai green da golf". Agron. J . 69:667–671.
Carrow, Marina militare, DV Waddington e PE Rieke. 2001. Fertilità del suolo del tappeto erboso e problemi chimici: valutazione e gestione . Chelsea, Michigan: Ann Arbor Press.
Dobbs, NA, KW Migliaccio, YC Li, MD Dukes e KT Morgan. 2014. "Valutazione dell'irrigazione applicata e dell'azoto lisciviato utilizzando diverse tecnologie di irrigazione intelligente sull'erba bahia ( Paspalum notatum )." Irrig. Sci. 32:193–203.
Erickson, JE, JL Cisar, GH Snyder, DM Park e KE Williams. 2008. "Un paesaggio con specie miste riduce la lisciviazione di azoto inorganico rispetto a un prato convenzionale di St. Augustinegrass?" Ritaglia Sci . 48:1586–1594.
Erisman, JW, MA Sutton, J. Galloway, Z. Klimont e W. Winiwarter. 2008. "Come un secolo di sintesi dell'ammoniaca ha cambiato il mondo". Naz. Geosci . 1:636-639. doi:10.1038/ngeo325.
Dipartimento dell'agricoltura e dei servizi ai consumatori della Florida. 2017. "Archivio dati sul tonnellaggio dei fertilizzanti". Accesso effettuato il 13 marzo 2017. http://www.freshfromflorida.com/Divisions-Offices/Agricultural-Environmental-Services/Business-Services/Fertilizer/Fertilizer-Manufacturers/Fertilizer-Tonnage-Data/Archive-Fertilizer-Tonnage-Data
Franzen, D., RJ Goos, RJ Norman, TW Walker, TL Roberts, NA Slaton, G. Endres, R. Ashley, J. Staricka e J. Lukach. 2011. "Studi sul campo e in laboratorio che confrontano l'urea di azoto-nutrisfera con l'urea nel Nord Dakota, nell'Arkansas e nel Mississippi". J. Pianta Nutr . 34:1198–1222. doi:10.1080/01904167.2011.558162.
Galloway, JN, FJ Dentener, DG Capone, EW Boyer, RW Howarth, SP Seitzinger, GP Asner, CC Cleveland, PA Green, EA Holland, DM Karl, AF Michaels, JH Porter, AR Townsend e CJ Vorosmarty. 2004. "Cicli dell'azoto: passato, presente e futuro". Biogeochimica 70: 153–226. doi:DOI 10.1007/s10533-004-0370-0.
Galloway, JN, AR Townsend, JW Erisman, M. Bekunda, ZC Cai, JR Freney, LA Martinelli, SP Seitzinger e MA Sutton. 2008. "Trasformazione del ciclo dell'azoto: tendenze recenti, domande e potenziali soluzioni". Scienza 320: 889–892. doi:10.1126/science.1136674.
Goos, RJ 2011. Additivi fertilizzanti azotati, quali funzionano? Conferenza sulla fertilità del suolo dell'industria dell'estensione del centro-nord, Des Moines, IA. 16-17 novembre.
Guertal, EA e JA Howe. 2012. "Lisciviazione di nitrati, ammonio e urea nella bermudagrass ibrida influenzata dalla fonte di azoto". Agron. J . 104: 344–352.
Guillard, K. e KL Kopp. 2004. "Forma di fertilizzante azotato e lisciviazione di nitrati associata dal tappeto erboso della stagione fresca". J.Ambiente . Qual. 33:1822–1827.
Havlin, JL, JD Beaton, SL Tisdale e WL Nelson. 1999. Fertilità e fertilizzanti del suolo: un'introduzione alla gestione dei nutrienti . 6a ed. Fiume Upper Saddle, NJ: Prentice Hall.
Janzen, HH e JR Bettany. 1986. "Influenza del tiosolfato sulla nitrificazione dell'ammonio nel suolo". Sci del suolo. Soc. Sono. G. 50:803–806.
Katz, BG, DW Griffin, PB McMahon, HS Harden, E. Wade, RW Hicks e JP Chanton. 2010. "Il destino dei contaminanti trasportati dagli effluenti sotto i campi di drenaggio delle fosse settiche sovrastanti una falda acquifera carsica". J.Ambiente. Qual. 39:1181–1195. doi:10.2134/jeq2009.0244.
Malzer, GL 1989. "Incorporazione di inibitori della nitrificazione con urea e nitrato di urea-ammonio per mais irrigato". Fert. Ris. 18:141–151.
Malzer, GL, KA Kelling, MA Schmitt, RG Hoeft e GW Randall. 1989. "Prestazioni della diciandiammide negli stati del centro-nord". Comune. Suolo. Sci. Pianta anale. 20:2001–2022. doi:Doi 10.1080/00103628909368198.
Mancino, CF, WA Torello e DJ Wehner. 1988. "Perdite da denitrificazione da zolle di bluegrass del Kentucky". Agron. G. 80:148–153.
McGroary, P., TW Shaddox, JL Cisar, JB Unruh e LE Trenholm. 2017. "Fabbisogno annuale di azoto dei prati di Bahiagrass mantenuti in climi subtropicali". interno Tappeto erboso. Soc. Ris. Gv 13:1–9. doi:10.2134/itsrj2016.05.0420.
Morton, TG, AJ Gold e WM Sullivan. 1988. "Influenza dell'irrigazione eccessiva e della fertilizzazione sulle perdite di azoto dai prati domestici". J.Ambiente. Qual. 17:124–130.
Programma nazionale di deposizione atmosferica. 2015. https://nadp.slh.wisc.edu . Accesso effettuato il 10 febbraio 2023.
Nieder, R., DK Benbi e HW Scherer. 2011. "Fissazione e defissazione dell'ammonio nei suoli: una revisione". Biol. Fert. Suoli 47: 1–14. doi:10.1007/s00374-010-0506-4.
Petrovic, AM 2004. "Fonte di azoto e impatto temporale sulla lisciviazione dei nitrati dal tappeto erboso". Acta Hortic. 661: 427–432.
Pye, VI, R. Partrick e J. Quales. 1983. Contaminazione delle acque sotterranee negli Stati Uniti. Filadelfia, Pennsylvania: Univ. della Pennsylvania Press.
Sartain, JB 1985. "Effetto dell'acidità e della fonte N sulla crescita e sull'accumulo di paglia della bermudagrass tifgreen e sulla ritenzione dei nutrienti nel suolo". Agron. Gv 77:33–36.
Sartain, JB 2008. "Influenza comparativa della fonte di N sulla lisciviazione di N e sulla qualità, crescita e assorbimento di N dell'erba di Sant'Agostino". Sci del raccolto del suolo. Soc. Florida 67:43–47.
Schmidt, CA e MW Clark. 2012. "Efficacia di un muro di denitrificazione per trattare carichi di nitrati costantemente elevati". Eco. L'Ing. 42: 203–211. doi:10.1016/j.ecoleng.2012.02.006.
Shaddox, TW 2001. "Il destino dell'azoto durante la crescita del fairway di un campo da golf in diverse pratiche di gestione dell'azoto e intensità di irrigazione." Tesi di master, Università della Florida, Gainesville, FL.
Shaddox, TW e JB Sartain. 2001. "Il destino dell'azoto durante la crescita del fairway di un campo da golf in diverse pratiche di gestione dell'azoto". Sci del raccolto del suolo. Soc. Florida 60:59–63.
Shaddox, TW, JB Unruh e LE Trenholm. 2016a. "Lisciviazione di nitrati dall'azoto solubile applicata all'erba di Sant'Agostino 'Floratam' e al centopiedi comune durante la dormienza." Ritaglia Sci. 56:837–844. doi:10.2135/cropsci2015.02.0104.
Shaddox, TW, JB Unruh, LE Trenholm, PC McGroary e JL Cisar. 2016b. "Tasso di azoto richiesto per un'erba di Sant'Agostino accettabile e la lisciviazione di nitrati associata." Ritaglia Sci. 56:439–451. doi:10.2135/cropsci2015.04.0226.
Smil, V. 2001. Arricchire la terra: Fritz Haber, Carl Bosch e la trasformazione della produzione alimentare mondiale . Cambridge, Massachusetts: MIT Press.
Snyder, GH, BJ Augustin e JM Davidson. 1984. "Irrigazione controllata da sensori di umidità per ridurre la lisciviazione di N nel tappeto erboso di bermudagrass". Agron. G. 76:964–969.
Starr, JL e HC Deroo. 1981. "Il destino del fertilizzante azotato applicato al tappeto erboso". Ritaglia Sci. 21:531–536.
Stiegler, JC, MD Richardson e DE Karcher. 2011. "Assorbimento fogliare di azoto in seguito all'applicazione dell'ureaa per mettere specie di tappeto erboso verde". Ritaglia Sci . 51:1253–1260. doi:10.2135/cropsci2010.06.0377.
Strand, L. 1998. "Remineralizzazione e defissazione dell'azoto nel suolo". Accesso 21 novembre 2017. http://www.vaxteko.nu/html/sll/slu/ex_arb_vaxtnaringslara/EVN108/EVN108.HTM
Sullivan, WM, ZC Jiang e RJ Hull. 2000. "Morfologia della radice e sua relazione con l'assorbimento di nitrati nel bluegrass del Kentucky". Ritaglia Sci. 40: 765–772.
Telenko, DEP, TW Shaddox, JB Unruh e LE Trenholm. 2015. "Lisciviazione dei nitrati, qualità del tappeto erboso e tasso di crescita dell'erba di Sant'Agostino 'Floratam' e del centopiedi comune." Ritaglia Sci . 55: 1320–1328.
Trenholm, LE e JB Unruh. 2005. "Risposta del tappeto erboso nella stagione calda ai tassi e alle fonti di fertilizzanti". J. Pianta nutriente. 28: 991–999.
Trenholm, LE, JB Unruh e JB Sartain. 2012. "Lisciviazione dei nitrati e qualità del tappeto erboso nelle consolidate piante 'Floratam' St. Augustinegrass e 'Empire' zoysiagrass." J.Ambiente. Qual. 41:793–799.
Warneke, S., LA Schipper, MG Matiasek, KM Scow, S. Cameron, DA Bruesewitz e IR McDonald. 2011. "Rimozione dei nitrati, comunità di denitrificanti ed effetti negativi in diversi substrati di carbonio da utilizzare nei letti di denitrificazione". Risoluzione dell'acqua 45:5463–5475. doi:10.1016/j.waters.2011.08.007.
Wherley, BG, W. Shi, DC Bowman e TW Rufty. 2009. "Il destino del (15) N-nitrato applicato a un sistema di bermudagrass: profili di assimilazione nelle diverse stagioni". Ritaglia Sci. 49:2291–2301.
Young, NG 2015. "Acclimatazione del tappeto erboso della stagione calda per evitare la siccità in risposta al lieve deficit idrico del suolo ricorrente e alla fertilizzazione con azoto". Dottorato di ricerca Diss., Università della Florida, Gainesville, FL.


Aggiungi commento
Commenti